一般来说,如果所受外界压力不变,大多数物体的体积都有热胀冷缩的性质,在温度降低时,构成物质的分子或原子会逐渐安定下来,彼此逐渐接近,导致密度变大体积变小,相反温度升高时,密度变小体积增大。当然也有例外,如锑、铋、液态铁等物质在正常条件下恰好与上面的情况相反。
而水则是热胀冷也胀,实验证明,0℃的水加热到4℃时,其体积会缩小,在4℃时密度最大、体积最小,当温度超过4℃之后,体积随温度的上升而增加。水在0℃~4℃的阶段“冷胀热缩”的现象,通常称为反常膨胀。
冰和水的微观结构

科学家们普遍认为水的反常膨胀跟水分子的特殊排列有关。水分子是由两个氢原子和一个氧原子组成的。氧原子是中心原子,分别以一对共用电子与两个氢原子结合。
氢原子与氧原子结合成H-O共价键,O-H键是一个强极性键,使共用电子偏向于的氧原子一端,这样一来两个氢原子一端就带有部分的正电荷,会对附近另一水分子中的负电性较大氧原子产生一种结合力,这种结合力就是氢键。H-O共价键和氢键都具饱和性和方向性特征。饱和性是指一个电子与另一个电子配对以后就不能再与第三个电子成对。方向性是指在某一特定的方向上形成共价键,组成稳定结构。
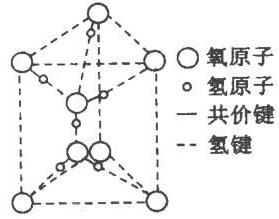
这样每个氧原子周围有四个氢原子,两个氢原子距氧原子较近,以共价键结合,另外两个氢原子距氧原子较远,以氢键相连,形成稳定的四面体结构。水分子之间的特殊微观结构导致其显示出特有的性质。
除了单分子H2O外,水中还有这些简单分子结合而成的较复杂的(H2O)n(n可以是2、3、4……)分子集团。这种由简单分子结合成较复杂的分子集团而不引起物质化学性质改变的过程,称为分子的缔合,相反的过程称为离解。
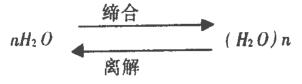
缔合是放热过程,离解是吸热过程,所以在温度降低时缔合程度较高(n增大),温度升高时,水的缔合程度降低(n减小)。
在水的缔合分子中,由于在双水分子中两个分子正负极互相吸引,故结合最紧密,所占体积最小,而三水分子中三个分子首尾相连,并架成三角形,所占空间较大。由此可见,水中的双水分子越多,则水的密度就越大。
升温过程中的结构变化
当温度降到0℃时,水结成冰,这时全部水分子缔合在一起,形成一个巨大的群体。由于氢键的饱和性和方向性,分子有规则的排列形成存在着较大空隙的空旷结构。
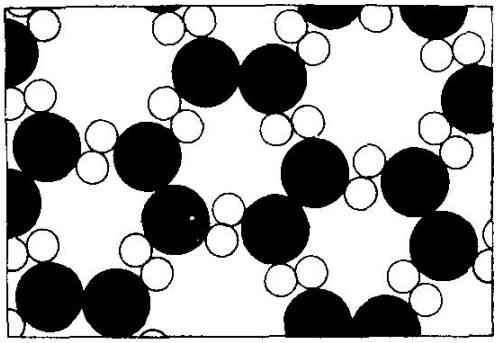
在温度未达到0℃之前,原子只在平衡位置附近作微小振动,能量增加,服从一般固态物质的热膨胀原理。当温度上升达到0℃时,晶体中部分原子的无规则动能足以使部分氢键断裂,空旷点阵结构逐渐瓦解为多分子集团,具有了流动性,固态转化为液态。由于分子集团间的杂乱排列,且集团间距离明显减小,因此,冰在熔解时体积要缩小。好比木材架空堆放时,占空间较大,拆散木架,将木材分别整齐堆放时,占有空间总体积变小。

继续加热0℃的水,多分子集团逐渐瓦解为三分子集团、双分子集团或单分子集团,在水温上升的过程中,一方面氢键不断地断裂,形成大量的小分子集团和单个水分子,这些小分子集团可以任意排列和运动,而且单个水分子可以嵌在大的多分子集团中间,使结构空隙更小,水分子之间更加紧密,水的密度增大。另一方面水分子的热振动动能增大,使分子间距增大,密度减小。水的密度受这两方面因素的共同影响。
在水温由0℃到4℃的过程中。由于水分子集团的氢键断裂引起的水密度增大的作用比热振动引起水密度减小的作用更大,所以在这个过程中,水的密度随温度的升高增大、体积减小,为反常膨胀。
在4℃时,水中的多聚分子大部分以双聚分子的形式存在,此时排列最为紧密,体积最小,密度最大。
水温超过4℃时,随着水温的升高,氢键进一步被破坏,多分子集团越来越少,单分子越来越多,氢键断裂引起的影响比热振动的影响小,所以在水温由4℃继续升高的过程中,水的密度随温度的升高减小、体积增大,即呈现热胀冷缩现象。
这样,热振动使分子间距扩大和断键使集团间距缩小两种相反的竞争机制,使得水在0℃~4℃之间有着反常膨胀的特性。4℃时,两种相反的机制几乎达到平衡,密度最大。4℃~100℃时表现为正常膨胀现象。
水的反常膨胀对自然界的作用

由此可见氢键在反常膨胀中的作用是非常重要的。实验发现,水在各种温度状态下都存在着不同程度的氢键。0℃以下结成六角晶系的冰,这时氢氧分子全部通过氢键连结,冰融化时,空旷结构瓦解,有15%左右的氢键断裂,在20℃以下,水中的氢键大约还保留了一半,即使在沸点水中也有可观数量的氢键。
氢键断裂需要较大能量,当冰变为水的过程中,仅就氢键断裂就能够使水有很高的热容(物体升高/降低单位温度时所吸收/放出的热量)。如此大的热容量对地球上环境温度的变化起着重要的调控作用,防止了温度的骤变,提供了适合人类生存的环境。
水的反常膨胀特性,对于水中的生物也具有重要的意义。寒冬到来时,水体表面自然冷却降温,密度增大下沉,下层的暖水上升,上下层不断地交换形成对流,整个水体的水温逐渐降低直到水温全部到达4℃为止。
气温继续下降,此时表层水温度下降密度反而减小,不再下沉产生对流,那么最冷的水保持在最上面,继续冷却就在顶层发生结冰。冰层因密度小浮在水上层,水深处仍是4℃左右。
水面冰封之后,水体就完全依靠热传导方式来进行热传递,由于水的导热系数小,持续冻结的速度是比较缓慢的,导致冰层不能快速向下生长,河流湖泊等较深的水体在有限的冬季里不会全部冻结。表层冰盖反倒成了天然防寒屏障,为水中生物提供了安全越冬的条件。
如果水也像其它物质一样始终保持热胀冷缩特性的话,在冷却和冻结时将不断收缩,冻结就会从最底部开始向上延伸,这样一来,大部分经受不住冰冻的动植物就无法越冬了。
当然水的冷胀现象也会带来危害,冬天若不注意防寒,水的冻结冷胀会使供水管道、汽车水箱等破裂,一些不耐寒的植物会由于细胞中的水冻结而胀破,发生冻害。公路、铁路若雪水渗入缝隙或路基中,再结冰可能使缝隙加大、路基松动产生危险隐患。水的反常膨胀特性,也是造成山岩崩裂、加速山体风化的重要物理原因。

 版权声明
版权声明