对元素的追问
化学诞生于人们对世界的追问,世界万物是由什么基本物质构成的?这些最基本的物质又是怎样变成万物世界的?元素就是在追问过程中获得的答案。无论是东方还是西方,元素的概念古已有之。但由于认识的元素较少以及科技水平发展的限制,人们对元素的认识都是孤立的单个“点”型元素研究。所谓的排列也是按价值、利用率或发现早晚排序的。这种排列没有任何“化学性质”的因素。
1869年俄国化学家迪米特里·门捷列夫经过长时间的分析、比较与综合,制作出系统的化学元素周期表,把当时已知的63种元素全部列入表内。元素周期表把构成万物的基本元素组成了一个相互联系的完整体系,简单清晰却非常深刻地揭示出物质世界的内在规律。虽然我们将元素周期表的创造归功于门捷列夫,但对于元素周期表的研究,门捷列夫不是第一人,也不是最后一人。元素周期表的演进,凝聚了一代又一代科学家的智慧。
几代科学家的成果积累
法国化学家安东尼·拉瓦锡首次将元素定义为基本物质,并于1789年出版了第一个元素表,为近代化学的发展奠定了基础。1803年,英国化学家道尔顿为了解释化学实验现象,创立了一种新的原子理论。他还发表了第一张原子量表,为后人测定元素原子量奠定了基础。1862年,法国地质学家尚库尔图瓦斯发表了一个被称为“地螺旋”的周期律方案,他是第一个看到元素周期性的科学家,他还发现,类似的元素是按照原子量周期性出现的。1864年,英国化学家约翰·纽兰兹注意到,如果元素按原子量排列,到了第8个元素就与第1个元素性质相似,即元素的排列每逢8就出现周期性。

约翰·道尔顿的元素列表
1860年在德国召开的第一次国际化学家代表大会,是元素周期表发展历史上的一个重要节点。会议上解决了许多重要的化学问题,最终确定了“原子”“分子”“原子价”等概念,并为测定元素的原子量奠定了坚实的基础。这次大会也对门捷列夫形成周期律的思想产生了很大的影响。此后,门捷列夫花了几年功夫潜心研究和收集元素数据,进行元素分类的试验。终于在1869年创造出了元素周期表。门捷列夫在周期表中发现的奥秘就是元素的周期性。随着原子质量的增加,元素的化学性质并非一直变化,而是间隔一段出现重复。类似的元素总要“鱼贯”地排成一队或一族。自此,乍看杂乱无章的物质世界,显示出了惊人的统一性。
给未知留出了可能性
门捷列夫是按照原子量(严格的说法应为相对原子质量或原子序数)从轻到重对元素进行编排,而非现代周期表的依据质子数量排列。许多年后,科学家们逐渐查出有11种元素的原子量测定得不准确,但门捷列夫当时无从得知,因为在门捷列夫的时代,给原子称重是很难的。加上对物质化合价的估计,通常可以产生2到4倍的结果。所以,有些元素并没有站在应该站的位置上。根据自己的理论,门捷列夫指出当时测定的某些原子量的数值有误,大胆地修正了一些元素的原子量,后来的研究结果证明他是正确的。

门捷列夫的元素周期表中留出的空格和预测
门捷列夫还意识到某些元素是缺失的,还有待被发现,因此在元素周期表上留下了空格。他利用空格让元素站到各自应站的位置上,避免了周期律的破坏,也为未知事物留出了空间。例如,在铝旁边有一个留给某种未知金属的空间。门捷列夫预言,它的原子质量为68,密度为每立方厘米6克,熔点很低。六年后,法国化学家保罗·埃米尔·勒科克·德布瓦博德兰分离出了镓,它的原子质量为69.7,密度为每立方厘米5.9克,熔点很低——门捷列夫留下的空缺被完美地填补了。
门捷列夫元素周期表取得最终的胜利是在收编“惰性一族”后。一开始,门捷列夫的元素周期表是没有为惰性气体预留空间的。在1894年以及其后的几年中,拉姆齐等科学家相继发现了氩等稀有气体元素。门捷列夫对周期表系统进行了一次最大的修改,专门为惰性气体设置了一个新专栏。1906年,门捷列夫在生前最后一版《化学原理》一书中把“惰性一族”排进了元素周期表,至此元素周期表在列上算是完整了。
对周期表排列方式的探索
乍一看,门捷列夫的表格不太像我们熟悉的元素周期表。一方面,现代的周期表上有一堆门捷列夫忽略(以及没有留出空间)的元素。另外,这张表的排列方式也与现代版本不同。把门捷列夫的表格旋转90度,就能看出它与现代版本的相似之处了。
事实上,在门捷列夫的元素周期表问世之后,科学家们对元素的其他排列和分布进行过大量实验。在将门捷列夫的表格进行这次永久的90度翻转之前,就有人尝试过一些古怪而奇妙的扭转了。
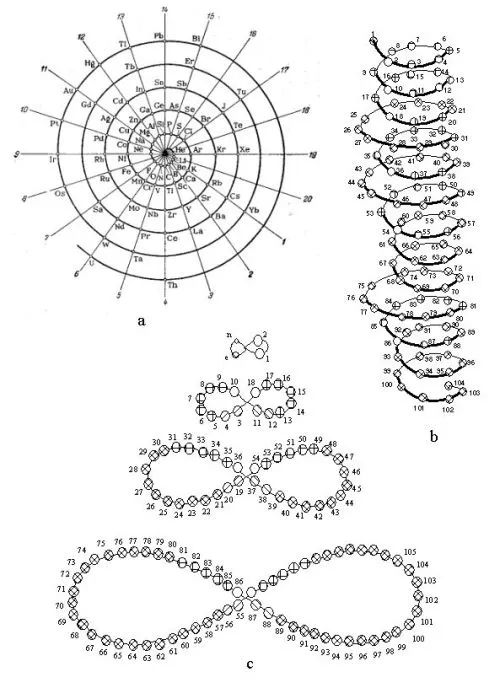
(a)海因里希·鲍姆豪尔的螺线形元素周期表;
(b)阿洛瓦斯·比列基提出的螺旋形元素周期表;
(c)亨利·巴塞特的“哑铃”设计。
一个特别引人注目的例子是海因里希·鲍姆豪尔于1870年发表的螺旋结构,它以氢元素为中心,元素随着原子质量增加呈螺旋式上升,每个轮辐(从中心到外围的直线)上的元素具有相同的属性。还有亨利·巴塞特在1892年提出的“哑铃”方案等等。
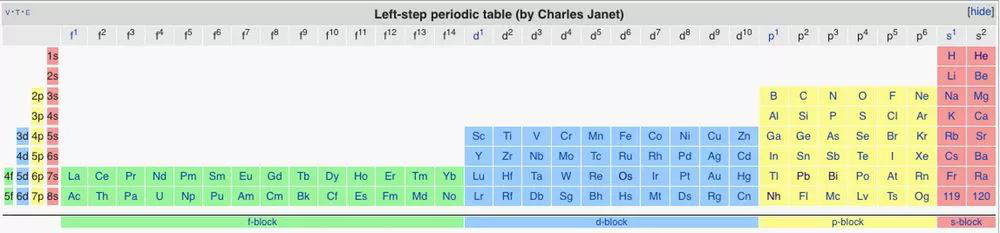
查尔斯·詹内特的左阶元素周期表
然而,到了20世纪初,这张表格就慢慢定型成了我们今天所熟悉的这种水平布局。特别有影响力的是查尔斯·詹内特的版本。他采用物理学家的方法,利用新发现的量子理论,建立了一个基于电子构型的布局。现代的元素周期表实际上是詹内特版本的直接演变。碱金属(以锂为首的第一主族元素)和碱土金属(以铍为首的第二主族元素)从最右边被移到了最左边,形成了一个非常宽的元素周期表。出于美学原因,f-区元素(指原子壳层最外层电子占据f-轨道,也就是镧系和锕系元素)通常被剪切下来,放到主表下面。这就是元素周期表演变到今天我们熟悉的样子的历程。
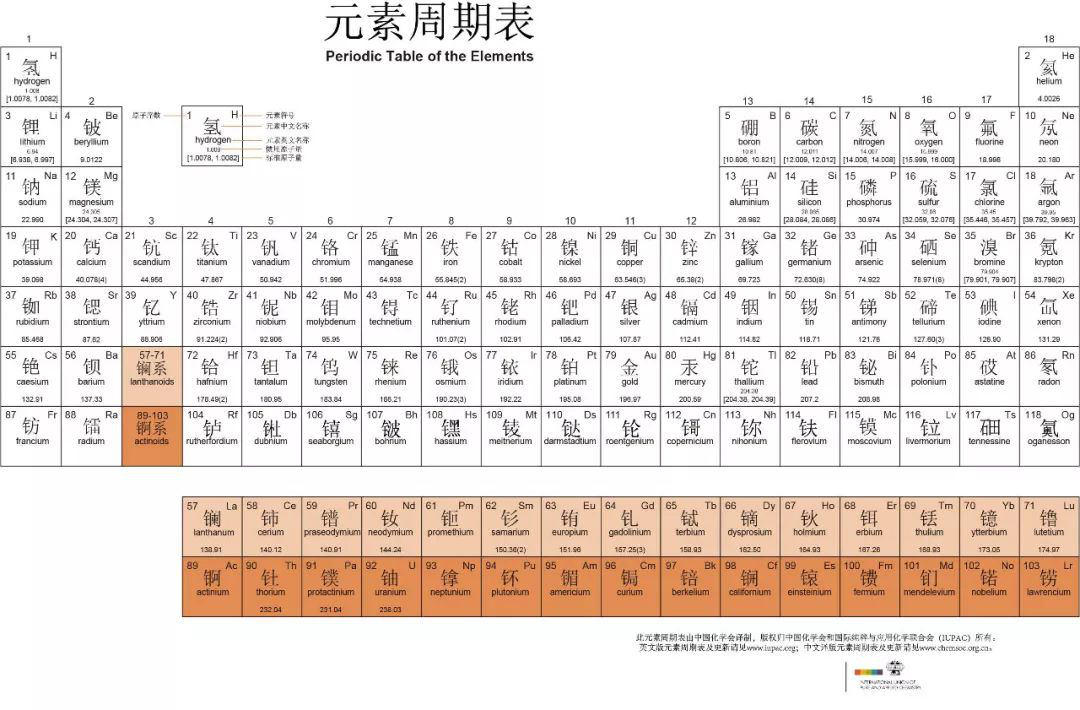
门捷列夫的元素周期表开辟了化学研究的一个崭新时代,奠定了现代元素研究的基础,随着现代化学的发展,科学家们开始利用周期表的规律,自己动手创造新元素。1937年,美国加州大学伯克利分校利用回旋加速器用氘原子核去“轰击”第42号元素钼,得到了锝,填补了第43号的位置,这是世界上第一个人造元素。
如今,元素家族成员不断扩大,2015年,IUPAC(国际纯粹与应用化学联合会)确认人工合成了113号、115号、117号和118号4个新元素。至此,发现并获得认可的化学元素已有118个,元素周期表第七周期被全部填满。但科学家们仍在为元素周期表开疆扩土。未来,对元素的探索不会止步,更多的奥秘仍有待发现。

 版权声明
版权声明